 東北大学の研究グループは,東京大学と共同で,がんの転移活性化因子の量を高精度で検出する方法を開発した(ニュースリリース)。
東北大学の研究グループは,東京大学と共同で,がんの転移活性化因子の量を高精度で検出する方法を開発した(ニュースリリース)。
がんにおいては,がん細胞が他の臓器へ転移し再発することが少なくない。乳がんについては,年間約7.2万人が新たに罹患し,約1.3万人が再発などの予後不良により亡くなっている。近年,HER2というタンパク質を標的とした抗がん剤が開発され,乳がんの治療成績が向上している。
しかし,HER2陽性患者は患者の一部(約15-20%)であり,大部分(約80-85%)の患者はHER2陰性となっている。HER2陰性患者の内,約65-70%の患者はホルモン受容体陽性であり,ホルモン療法を受けられるが,残りの10-15%の患者はHER2およびホルモン受容体ともに陰性であるため,効果的な診断マーカーや治療薬が乏しく,予後が悪いことが知られている。
がんの予後の悪化に関係する因子は,診断マーカーになると同時に,治療薬開発の標的にもなる。研究では,診断や治療の標的因子として,がん転移に関係するタンパク質PAR1に注目した。
PAR1が活性化されると,がん細胞の運動能や浸潤能を高め,がん細胞の転移能を増加させる。PAR1の活性化に必要な部分を認識する抗体(PAR1抗体)を作製し,ヒト乳がん由来の培養細胞で解析した結果,PAR1抗体がPAR1に結合すると,PAR1の活性化が阻害され,がん細胞の運動能や浸潤能が著しく抑制されることが明らかになった。したがって,PAR1抗体を改良(ヒト化抗体)すれば,がん転移を抑制する抗体医薬になり得る。
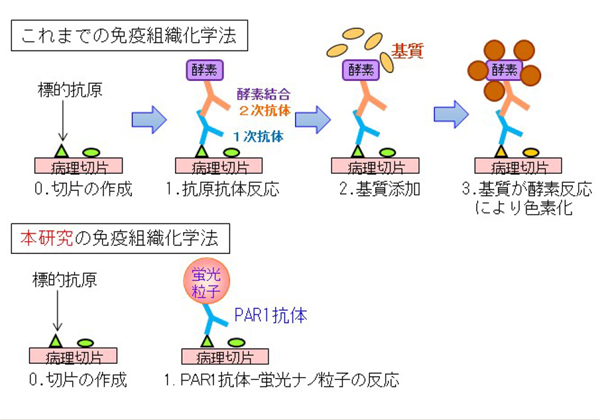
つぎに,このPAR1抗体を用いて,がん組織の新規診断法を開発した。これまで,抗がん剤の有効性や術後の予後を診断するために,がんの組織切片に対する酵素発色反応を利用した方法(免疫組織化学法)が用いられてきた。これは,がん組織切片に対し,酵素を結合した標的因子特異的な抗体を反応させ,酵素反応により茶色い色素を発色させることで,がん組織の形態と性質を同時に調べる方法。
しかし,この方法は,酵素反応による発色強度が温度,時間,基質量に左右され,標的因子の存在量の定量性(数値化)が不十分だった。定量性が低いと,がんの診断精度が悪くなるため,定量性の高い方法の開発が大きな課題となっていた。
研究では,この課題を解決するため,蛍光ナノ粒子の1粒子イメージングと画像解析を組合せた新規の検出方法の開発を行なった。まず,PAR1抗体と蛍光ナノ粒子を結合させた「PAR1抗体-蛍光ナノ粒子」を作製し,この蛍光マーカーをヒト乳がん組織へ反応させた。その後,撮影した蛍光画像を差分画像解析という方法を用い,蛍光マーカー由来の信号のみを取り出すことに成功した。
その後,蛍光信号画像において蛍光ナノ粒子の信号を1つずつ数えることで「PAR1抗体-蛍光ナノ粒子」の数を正確に測定することができた。この粒子数はPAR1抗体が認識するPAR1の存在量を高精度で表しているため,高い定量性を実現することになる。
さらに,「PAR1抗体-蛍光ナノ粒子」を用いた本方法により,HER2陰性乳がん患者の予後診断を試みた。乳腺正常組織,5年以上無再発の乳がん組織,3年以内再発の乳がん組織,の3種類のヒト組織に存在するPAR1量を調べた結果,PAR1量は3年以内再発の乳がん組織で最も高く,またPAR1量と手術後再発までの期間に強い相関性があることを見出すことに成功した。
研究グループではこの成果について,PAR1抗体の再発予防治療薬(抗体医薬)への応用を期待させるとともに,「PAR1抗体-蛍光ナノ粒子」で検討する症例数を増やし評価基準の確度を向上させることで,がん患者の新たな予後予測診断法へ発展することが大いに期待されるものとしている。
関連記事「慶大,がん転移を促進する新たな仕組みを解明」「東大,スプレーするだけでがんを光らせる蛍光試薬を開発」「阪大、 乳がん細胞の逃亡を抑制する遺伝子を発見」




























